مقدمهای بر سلولهای الکتروشیمیایی و باتری فلز-هوا
مقدمهای بر سلولهای الکتروشیمیایی و باتری فلز-هوا
افزایش روزافزون آلودگیهای زیست محیطی و گرمایش بیسابقهی جهانی به دنبال استفاده از سوختهای فسیلی و البته محدودیت این منابع سبب افزایش توجه کشورهای مختلف دنیا به حوزهی انرژیهای تجدیدپذیر و پاک و نیز اختصاص بخش کلانی از بودجهی پژوهشی آنها به این بخش شده است.
انرژی الکتریکی میتواند یکی از بهترین جایگزینها برای سوختهای فسیلی در آینده باشد. روشهای تجدیدپذیر و پاک متعددی برای تولید انرژی الکتریکی وجود دارد که از آن جمله میتوان به توربینهای آبی در نیروگاههای برق-آبی، توربینهای بادی در نیروگاههای بادی و صفحات خورشیدی اشاره کرد که هرکدام مزایا و معایب خود را دارند.
یکی از روشهای نسبتا پاک و تجدیدپذیر برای تولید انرژی الکتریکی استفاده از سلولهای الکتروشیمیایی است. این سلولها که در اصطلاح عام به باتری معروفند، انواع مختلفی دارند و ما قصد داریم در این مقاله به معرفی باتری فلز-هوا بپردازیم.
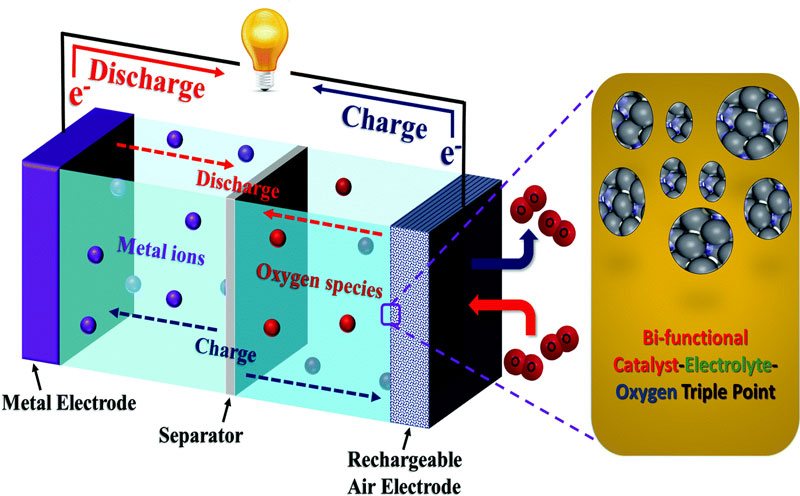
همانگونه که در شکل فوق میبینید، باتریهای فلز هوا دارای یک آند فلزی از جنس آلومینیوم، منیزیم، روی، لیتیوم یا فلزات دیگر یا آلیاژی از این فلزات و یک الکترولیت که میتواند محلولی آبی یا آلی یا نوعی جامد باشد، تشکیل شده است و از هوا به عنوان کاتد استفاده میکند. در این نوع از سلولهای الکتروشیمیایی، اکسیژن مولکولی موجود در هوا در مرز آند با الکترولیت با فلز واکنش داده و فلز را یونیزه میکند. سپس یونهای آزاد فلزی وارد محلول الکترولیت میشوند و جریان الکتریکی در باتری برقرار میشود. واکنشهای شیمیایی باتریهای هوا-فلز به صورت زیر رخ میدهند (در این مثال از روی به عنوان آند استفاده شده است):
مشخصات آند در باتری هوا-فلز
پتانسیل اکسیداسیون فلزهای مختلف با هم دیگر متفاوت است و بنابراین در هر باتری که، بسته به نوع کاربرد، از فلز خاصی به عنوان آند در باتریهای هوا-فلز استفاده میکنند. یکی از متغیرهای تأثیرگذار در انتخاب یک باتری هوا-فلز برای کاربردی خاص، انرژی ویژه است. در جدول زیر انرژی مخصوص چند نوع از باتریهای هوا-فلز آورده شده است:
| نوع آند باتری هوا-فلز | انرژی ویژه |
| آلومینیوم | ۲۷۹۶ وات بر کیلوگرم |
| منیزیم | ۲۸۴۰ وات بر کیلوگرم |
| روی | ۱۰۸۶ وات بر کیلوگرم |
| لیتیوم | ۳۴۵۸ |
مزایای استفاده از فلز به عنوان آند در سلولهای الکتروشیمیایی عبارتند از: چگالی بالای انرژی و وفور مواد اولیه برای ساخت. با ان حال، فعالیت فلزات ضعیف است و توانایی کمی در تخلیهی جریان دارند. یکی از انوع باتری هوا-فلز که دهههای اخیر توجهات زیادی را به خود جلب کردهاند، باتریهای لیتیوم-هوا هستند که انرژی مخصوص بالایی دارند ولی واکنشپذیری بالای لیتیوم در این باتریها میتواند خطرآفرین باشد.
پژوهشهای زیادی نیز روی باتریهای منیزیم-هوا نیز به دلیل منابع زیاد و دردسترس منیزیم، وزن پایین، سمینبودن و واکنشپذیری خیلی بالا و در عین حال، ایمن بودن، صورت گرفته است. این باتریها بیشترین ولتاژ نظری را در میان دیگر باتریهای هوا-فلز دارند. در جدول زیر میتوانید ولتاژهای نظر باتریهای هوا-فلز که در ساخت آنها از فلزات متفاوتی استفاده شده است ببینید.
| آند | ولتاژ نظری بر حسب ولت | ولتاژ عملی بر حسب ولت | انرژی ویژهی نظری
برحسب کیلووات بر کیلوگرم |
| روی | ۶۵/۱ | ۱ الی ۲/۱ | ۳/۱ |
| لیتیوم | ۹۱/۲ | ۴/۲ | ۱۳ |
| آلومینیوم | ۷/۲ | ۲/۱ الی ۶/۱ | ۱/۸ |
| منیزیم | ۱/۳ | ۲/۱ الی ۴/۱ | ۸/۶ |
همانطور که در جدول فوق میبینید، بیشترین ولتاژ نظری متعلق به باتریهایی است که در ساخت آنها از آند منیزیمی استفاده میشود، اما بیشتری ولتاژ عملی را باتریهای لیتیومی دارند. فلز روی نیز ضعیفترین آندها را میسازد ولی ارزان و فراوان است.
مشخصات کاتد در باتریهای هوا-فلز
مادهی اصلی که در باتری هوا-فلز نقش کاتد را ایفا میکند اکسیژن است ولی نوع جایگاه کاتد برای فراهم آوردن دسترسی اکسیژن به فلز به منظور انجام واکنشهای متعاقب، از اهمیت بالایی برخوردار است.
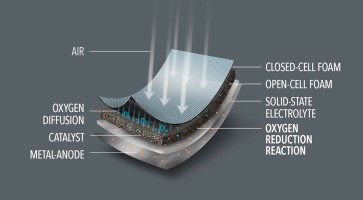
در شکل شماتیک فوق میتوانید ساختار کلی کاتد را در باتری هوا-فلز ببینید. هوا از منافذ یک پوشش آبگریز وارد کاتد میشود. پوشش آبگریز میتواند از جنس تفلون یا واکس باشدکه خواص آبگریزی دارند. سپس هوا از یک فوم که معمولا از جنس مخلوط پودر کربن ولکان یا استیلن و یک مادهی هیدروفوب است و لایهی انتشار گاز نامیده میشود عبور میکند.
لایهی بعدی در کاتد باتری هوا-فلز، کاتالیست است که کار آن افزایش سرعت واکنش احیای اکسیژن میباشد. از فلزات گرانبها، مواد دارای پایه کربنی، کمپلکسهای فلزی یا اکسیدهای فلزی گذرا به عنوان کاتالیست استفاده میشود. لایهی چهارم کاتد در این نوع باتریها لایهی جمعآوری جریان نام دارد. در جدول زیر میتوانید انواع کاتالیستهای مختلف در انواع باتری هوا-فلز را ببینید.
| دستهبندی کاتالیست | مواد مورد استفاده در کاتالیست | مشخصات کاتالیست |
| فلزات گرانبها | پلاتینیوم (Pt) | فعالیت کاتالیزوری: بالا نوع واکنش: چهار الکترونی
قیمت: زیاد |
| فلزات گرانبهای دیگر مثل پالادیوم (Pd)، طلا (Au)، نقره (Ag) | فعالیت کاتالیزوری: کمتر از Pt
قیمت: زیاد |
|
| اکسیدهای فلزی گذرا | اکسیدهای منگنز (MnOx)، اکسید کلسیم-منگنز (CaMnO3) و اکسید کبالت منگنز (CoMn2O4) | فعالیت: بالا در حد فلزات گرانبها
قیمت: پایین پایداری: بیشتر از فلزات گرانبها |
| مواد دارای پایهی کربن | کربن دارای تخلخل بالا، نانولولههای کربنی و گرافن | دسترسی: آسان
سازوکار واکنش: دو الکترونی |
| کمپلکسهای فلزی | آهن (III) تترامتوکسی فنیل پورفیرین (FeTMMP-C)،
کبالت تترامتوکسی فنیل پورفیرین (CoTMMP-C)، کبالت فتالوسیانین روی نانوذرات نقره روی یک پایه کربنی (CoPcF16@Ag/C) |
پایداری: بالا و قابل مقایسه با پلاتینیوم،
قیمت: کم |
قیمت بالا فلزات گرانبها مهمترین عامل محدودکنندهی استفاده از آنهاست. بهترین کاتالیست در میان کاتالیستهای گرانبها، پلاتینیوم است. اکسیدهای فلزی گذرا به دلیل قیمت پایین جایگزین مناسبی برای فلزات گرانبها هستند ولی پایداری پایینی دارند. مواد دارای پایهی کربنی نیز ارزان هستند ولی پایداری خوبی دارند. توجه داشته باشید که نانولولههای کربنی به شدت خطرناک و سرطانزا میباشند. کمپلکسهای فلزی نیز پایداری خوبی دارند و هزینهی آنها نیز خیلی پایین است و برخلاف نانولولههای کربنی، سمی نیستند.
ویژگیهای الکترولیت در باتریهای هوا-فلز
الکترولیت با هر دو الکترود باتری هوا-فلز تماس دارد و جریان الکترونها و یونها بین آنها را برقرار میکند. نوع الکترولیت به کار رفته در این باتریها به نوع فلز مورد استفاده برای ساخت آند و نوع کاتالیست مورد استفاده برای ساخت کاتد بیشترین وابستگی را دارد.
الکترولیت زمینهی انجام واکنشهای شیمیایی است و باید پایینترین مقاومت ممکن را برای باتری فراهم آورد تا باتری هوا-فلز بیشتری کارایی ممکن را داشته باشد. از مواد مختلفی به عنوان الکترولیت استفاده میشود. بعضی از این مواد دارای pH قلیایی هستند و بعضی نیز pH خنثی دارند.
محلولهای سدیم کلراید، هیدروژن کلراید، هیدروکسید سدیم، آمونیاک و هیدروکسید پتاسیم، الکترولیتهای معمول مورد استفاده در باتریهای هوا-فلز هستند. بیشترین ولتاژ (۷۲/۱ ولت) در بین باتریهای هوا-فلز، متعلق با باتری هوا-فلزی است که در آند آن از منیزیم و در الکترولیت آن از محلول سیدم کلراید استفاده شده باشد.
بعضی از انواع باتری هوا-فلز دارای داری یک مسیر جریان گردشی برای محلول الکترولیت میباشند و در نتیجه دسترسی الکترولیت به آند و کاتد بیشتر شده و از ایجاد حالت ژلهای در الکترولیت به دلیل استفادهی زیاد از باتری، جلوگیری میشود.
باتری های فلز-هوا در ایرانْ با سامانه سانیوا آشنا شوید






دیدگاه خود را ثبت کنید
تمایل دارید در گفتگوها شرکت کنید؟در گفتگو ها شرکت کنید.