راه حل باتری های فلز-هوا برای خودروهای برقی
حل چالش استفاده از خودروهای برقی درکشور با سانیوا(نسل جدید باتری ها)
امروزه براساس گزارش ها، بزرگترین چالش خودروهای برقی تامین و مداومت انرژی است. باتری های فلز-هوا با قابلیت های ویژه خود می توانند این مشکل را حل کنند. سانیوا نسخه ایرانی باتری های فلز-هواست.
این روزها بحث جایگزینی خودورهای برقی با خودروهای بنزینی بسیار مطرح هست.
اما برای ورود این فناوری به کشور ما و فراگیر شدن آن موضوعاتی وجود دارد؛ از جمله چالش جایگزینی با خودروهای بنزینی به علت پایین بودن قیمت سوخت در کشور، چالش های زیست محیطی، تامین انرژی و عدم پذیرش اجتماعی این خودروها در داخل کشور.
سوخت فسیلی ارزان در کشور، مانع اقبال عمومی به خودروهای برقی
درمورد امکان جایگزینی خودروهای برقی با خودروهای معمولی، با توجه به قیمت بسیار پایین سوختهای فسیلی در کشور و همچنین قیمت بالای تامین انرژی این خودروها شاید به راحتی نتوان آن ها را جایگزین خودروهای فعلی نمود.این در حالیست که کشور ما به علت تولید و استفاده از سوخت های فسیلی سهم بالایی در آلودگی های محیط زیستی دارد و باید به دنبال راه های نوین و پاک تامین انرژی بود.
تامین انرژی خودروهای برقی در طول مسیر
خودروی های برقی در حال حاضر به علت مداومت انرژی پایین باتری های به کار رفته در آن ها، نیاز به زیرساخت های شارژ در فواصل مشخص و کوتاهی دارند.
سال ها پیش با ورود خودروهای دوگانه سوز و گاز سوز به بازار نیز ما با چالش جایگاه های تامین انرژي مواجه شدیم و شاهد صف های طولانی و عدم وجود زیرساخت های مناسب برای آن ها بودیم. این درحالی اتفاق افتاد که زمان شارژ خودروهای گازسوز و بنزینی درحد چند دقیقه می باشد همچنین تاحدود زیادی زیرساخت های آن ها مشابه بود. با افزایش این زمان به چندین ساعت در خودروهای برقی و همچنین عدم وجود زیرساخت مشابه در گذشته، درباره این خودروها با چالش های بیشتری روبرو خواهیم شد. علاوه براین، در ایستگاه های شارژ برقی به علت وجود باتری های لیتیومی( باتری خودروهای برقی) در صورت عدم کنترل دما شاهد انفجارهای مهیبی خواهیم بود که خطر استفاده از این خودروها را افزایش می دهد.
در حال حاضر در کشور تنها یک ایستگاه شارژ برق وجود دارد که برای موتورسیکلت های برقی می باشد.
همچنین در کشورهای پیشرفته مانند آمریکا نیز تعداد این ایستگاه ها چندان نیست. در مجموع می توان گفت مسئله ایستگاه های شارژ و از سوی دیگر فواصل زمانی کوتاه برای شارژ مجدد از مهم ترین مسائلیست که صنعت خودروهای برقی را با چالش روبرو کرده است.
خودروهای برقی و چالش محیط زیست
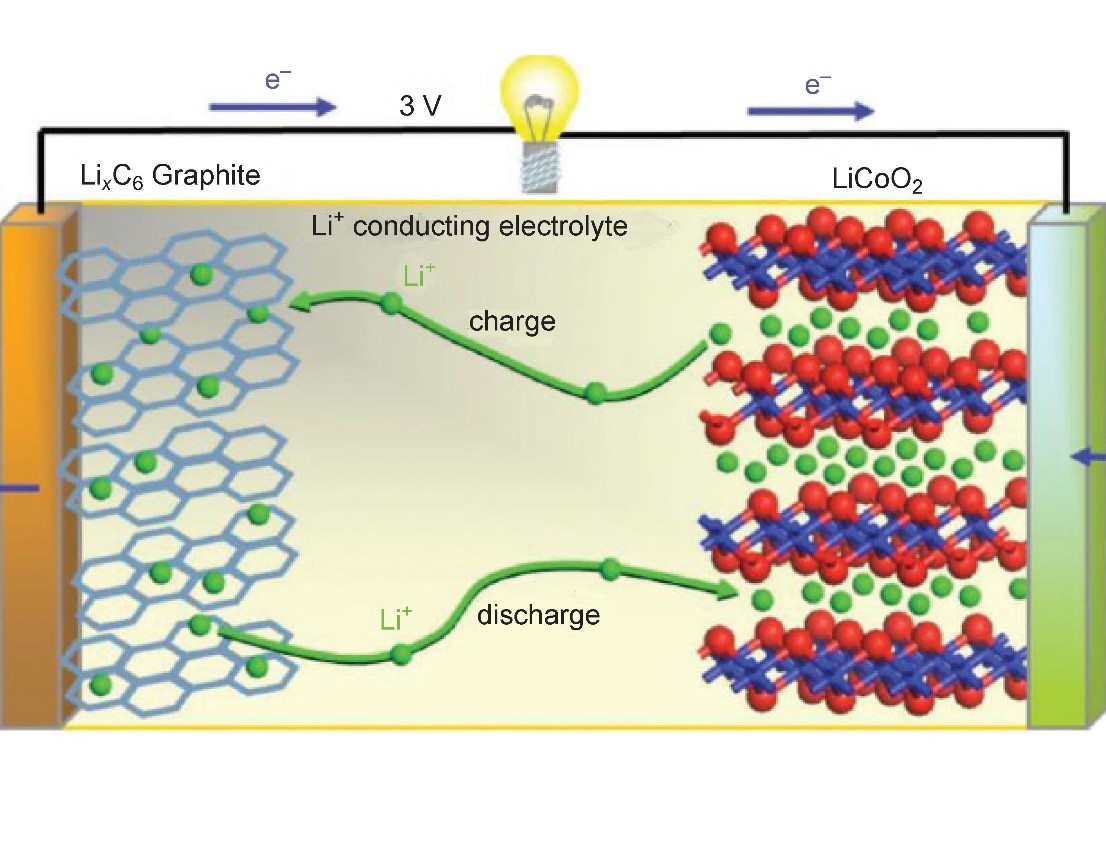
موضوع دیگری که درباره خودروهای برقی وجود دارد مسئله محیط زیست می باشد. در حال حاضر این خودروها از باتری های لیتیومی بهره میبرند که دارای آلودگی های محیطی بسیار می باشند و آسیب جدی به محیط زیست وارد می کنند. در حال حاضر یکی از مطرح ترین پروژه ها در دنیا بازیافت این باتری ها جهت کاهش آلودگی آن ها می باشد.
چالش مهم دیگر ورود این خودروها به ایران، بعد اجتماعی آن هاست
شاید بتوان گفت در کشورهایی همانند چین و ژاپن پذیرش فناوری های نوین و جایگزینی آن ها با نسل های قدیمی تر راحت تر انجام می شود و با اقبال عمومی مواجه می شود. اما در کشورهایی مانند ایران که هم اکنون نیز در برخی روستاها و شهرها از تجهیزات و خودروهای دو الی سه نسل قبل همچنان استفاده می شود، پذیرش ابزارها و تجهیزات نوین به ویژه خودروهای برقی و جایگزینی آن ها با مشکل روبرو شود.
این در حالیست که به علت وجود تعهد پاریس و جرایم سنگین در نظر گرفته شده، کشور موظف به کاهش آلودگی های زیست محیطی می باشد. در صورت عدم اجرا، کشور متقبل هزینه های سنگینی خواهد شد. جایگزینی خودروهای خودروهای برقی یکی از راه حل های این موضوع است.
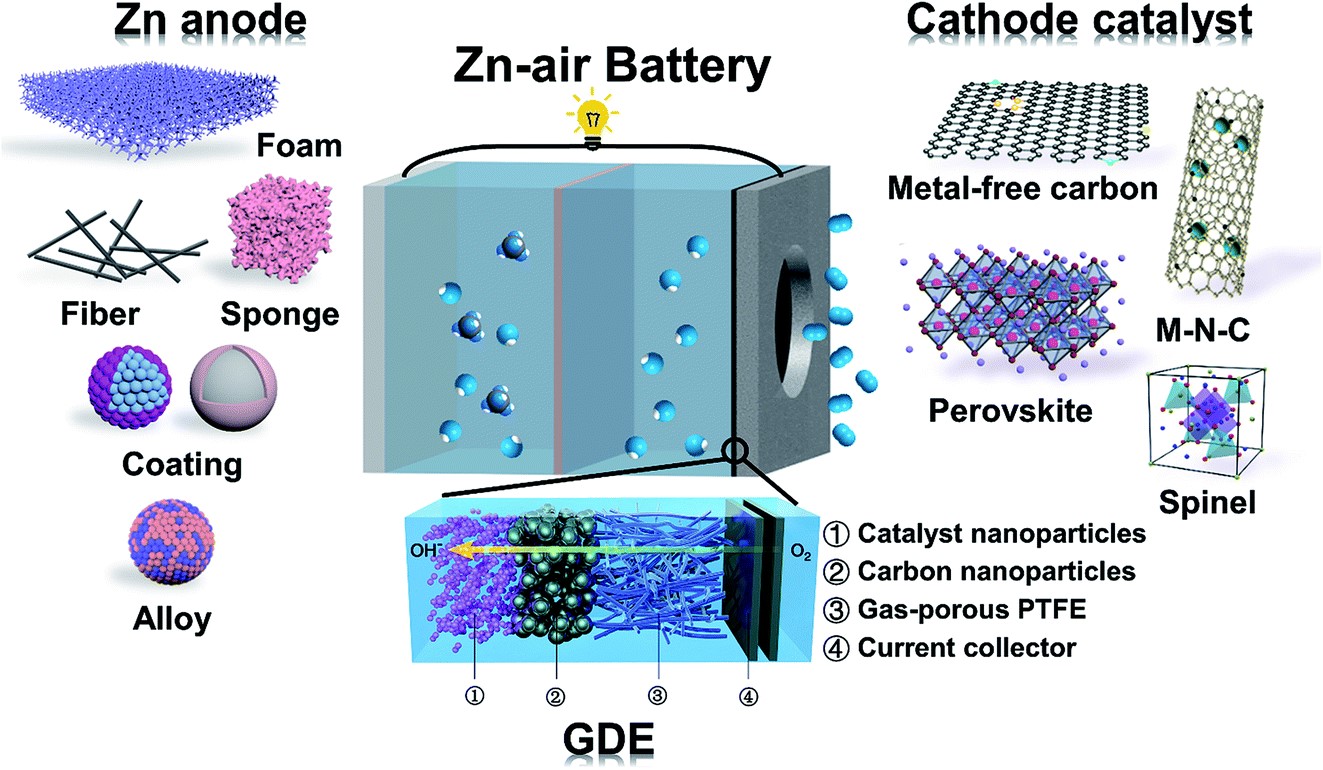
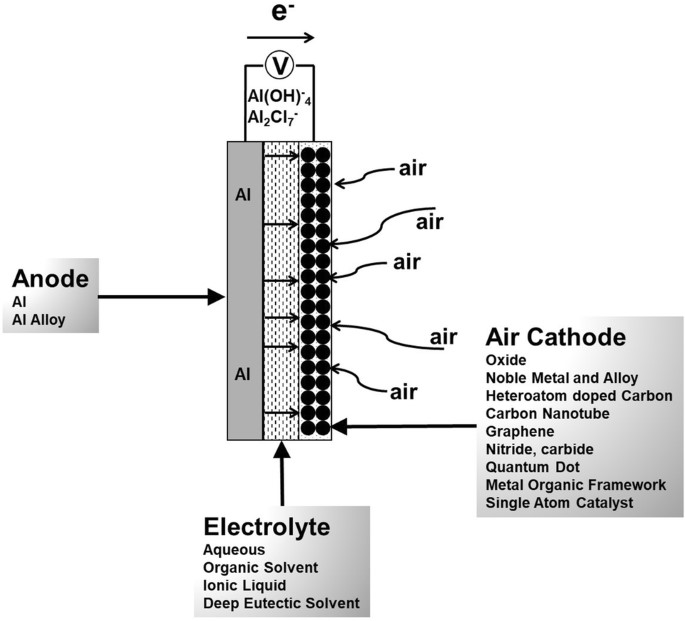
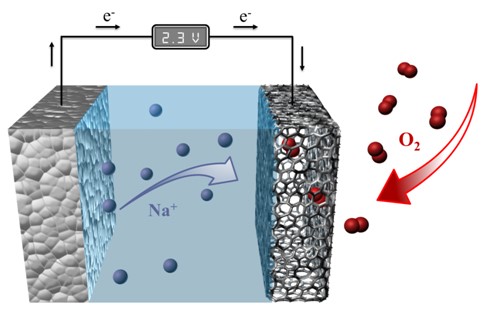
باتری های فلز-هوا ر اه حلی برای مشکلات خودروها
باتری های فلز-هوا به علت تفاوت نوع شارژی که با باتری های لیتیومی دارند(باتری های استفاده شده در خودروهای برقی) می تواند، فواصل زمانی شارژ مجدد خودروهای برقی را که در حال حاضر هر 300 کیلومتر با می باشد، به ۱۲۰۰ کیلومتر افزایش میدهد. در واقع کاربر در طول مسیر نیازی به شارژ مجدد خودروی خود نخواهد داشت.
همچنین شارژ این باتری ها با زیرساخت های موجود در کشور میسر است و نیازی به ایستگاه های شارژ مجزا و پیچیده ندارند و ایمن هستند.
از سوی دیگر در ساخت باتری های فلز-هوا و الکترولیت آن ها از موادی کاملا سازگار با محیط زیست استفاده شده است که باعث می شود این باتری ها آلودگی زیست محیطی نداشته باشند. همین امر سبب می شود تا استفاده از این باتری ها در خودورهای برقی، به نوبه خود با کاهش آلودگی های محیط زیستی به شکل قابل توجهی در انجام تعهدات معاهده پاریس نقش داشته باشد.
در واقع می توان گفت به طور کلی، در صورت تجاری سازی باتری های فلز-هوا بزرگترین چالش خودورهای برقی در دنیا که مسئله شارژ و مدوامت انرژی می باشد، حل خواهد شد و شرایط ورود این فناوری و استفاده از آن را در کشور بسیار آسان خواهد نمود.
در حال حاضر شرکت های بزرگی در دنیا مشغول تحقیق و توسعه این باتری ها می باشند که در ایران نیز به همت دانشمندان جوان کشورمان فناوری باتری های فلز-هوا در پروژه ای به نام سانیوا بومی سازی شده است.