باتری لیتیوم هوا(Lithium air battery) ویژگی ها، ساختار و انواع
مروری بر ویژگی ها باتری لیتیوم هوا
آنچه پیش رو دارید، به طور خاص بر بررسی ویژگی ها و اساس کار باتری لیتیوم هوا (Lithium air battery) متمرکز است؛ فرض بر این است خواننده، با اساس کار باتری فلز هوا و نحوه ی عملکرد و اجزاء آن و وجه تمایز آن از سایر باتری ها، آشنا است؛ در عین حال به صورت گذرا، ویژگی ها و اساس کار باتری لیتیم هوا، به عنوان یک باتری فلز هوا مرور خواهد شد.
ظرفیت ویژه انرژی
برای باتری های فلز هوا، یک ویژگی مهم با عنوان انرژی ویژه با واحد وات ساعت بر کیلوگرم تعریف می شود. این مقدار عبارت است از میزان انرژی الکتریکی بر حسب وات ساعت (و نه ژول) که هر گرم از باتری تامین می کند. واحد جرم در مخرج، بیانگر اندک بودن جرم نهایی باتری برای تامین میزان مطلوب انرژی بسیار مهم است. مصرف فلزات و الکترولیت و همچنین استفاده از باتری های فلز هوا در فناوری های حمل و نقل، بر اندک بودن ترجیحی جرم باتری تاکید دارد.
واقعیت آن است که باتری لیتیوم هوا در این ویژگی بی نظیر و زبانزد است. دست کم پیاده سازی های آزمایشگاهی گویای این مطلب است. فناوری باتری های فلز هوا، به سرعت در صدد رفع چالش هایی است که در مقابل باتری لیتیم هوا (Lithium air battery) وجود دارد.
مقایسه ی ظرفیت باتری
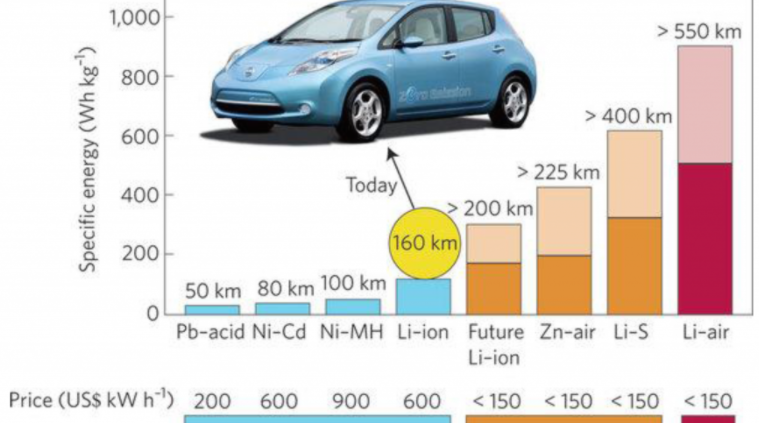
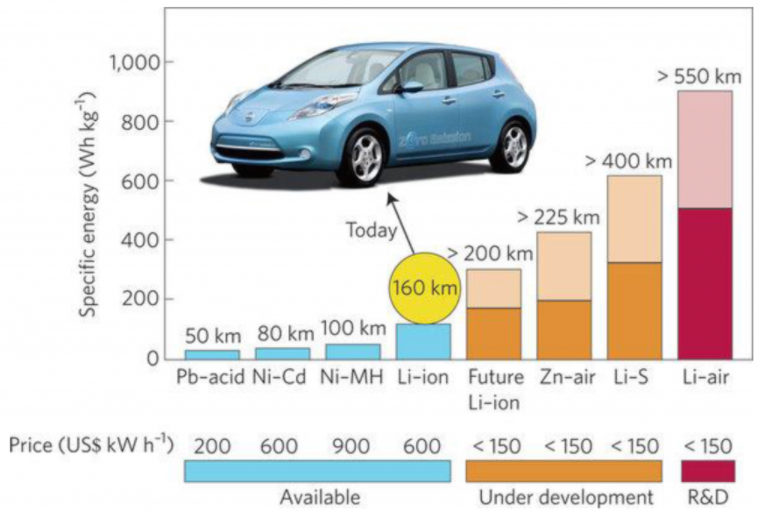
در شکل زیر (گراف مقایسه انواع باتری ها) گراف انرژی ویژه برای چندین نوع باتری ارائه شده است؛ این گراف گویای مطالب زیادی است. اولاً بیان می دارد ظرفیت انرژی برای انواع باتری قابل مقایسه با ظرفیت Lithium air battery نیست. به گونه ای که این ظرفیت برای باتری های اسید – سرب، نیکل – کادمیم، نیکل – متال هیبرید، لیتیوم – یون، به مقادیری کمتر از 200 رسیده است. در ویرایش در دست توسعه لیتیوم – یون به صورت بهینه سازی شده، باز هم این مقدار به 400 نمی رسد.
گراف مقایسه ی انواع باتری ها
حتی باتری فلز هوای مبتنی بر روی یا زینک، کمتر از 500 وات ساعت بر کیلوگرم ظرفیت ویژه دارد. این در حالی است که باتری لیتیوم هوا دارای ظرفیت در حدود 1000 واحد می باشد. گراف البته اذعان دارد باتری های تجاری شده که با رنگ آبی مشخص شده اند، به بلوغ کافی رسیده اند و برخی ویرایش های باتری لیتیوم-یون و باتری فلز هوای مبتنی بر روی، در دست توسعه و در حال پیشرفت مسیر تجاری سازی هستند. اما درباره ی باتری لیتیوم هوا موضوع در فاز تحقیق و توسعه (Research & Development) می باشد.
مقایسه ی مسافت طی شده
رابطه ی مشابهی نیز در گراف بین ظرفیت ویژه و مسافت طی شده با مقدار واحد و یونیک شارژ وجود دارد. این مقدار یونیک می تواند یک سیکل شارژ کامل، زمان مشابه شارژ یا … تلقی شود. باتری های تجاری شده، 50، 80، 100 و نهایتاً 160 کیلومتر طی مسافت خواهند داشت.
در گراف مقایسه انواع باتری ها وضعیت فعلی فناوری، که بلوغ باتری لیتیوم-یون و طی مسافت 160 کیلومتر است، بیان شده است. فناوری های در دست اقدام، این مسافت را به بازه ای بین 200 الی 400 کیلومتر می افزاید. اما انقلاب فناوری مبتنی بر باتری لیتیوم هوا، این مسافت طی شده را به 550 کیلومتر به عبارتی حدود 4 برابر سطح فعلی تکنولوژی خواهد رسانید.
مقایسه ی هزینه و قیمت باتری لیتیوم هوا
مطلب دیگر ارائه شده در گراف مقایسه انواع باتری ها، مبحث هزینه ی باتری است. باتری های بالغ شده تجاری سازی شده، برای تامین هر کیلووات ساعت، مقادیری بیش از 200 دلار الی 900 دلار، هزینه در بر خواهند داشت. این در حالی است که فناوری بر بالا بودن این هزینه برای کاربر اطلاع یافته و به عنوان قید طراحی و پیاده سازی .و حتی قید و شرط تحقیق و توسعه، سقف 150 دلار را برای هزینه ی تامین یک کیلو وات ساعت لحاظ نموده است.
تئوری تا تجاری سازی
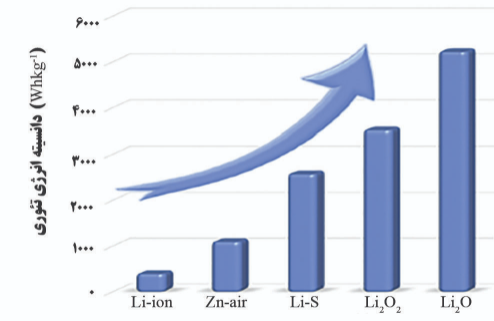
بیان ظرفیت انرژی ویژه ی باتری لیتیوم هوا، مختص یک منبع خاص یا یک تحقیق و پژوهش نیست؛ بلکه در منابع مختلف مشابه این گراف نمایی، که ظرفیت این باتری را در مقایسه با دیگر باتری ها غیر قابل مقایسه می کند، منتشر شده است. آنچه در شکل زیر نمایان است، اشاره ی صادقانه به تئوری بودن نتایج و غیر تجاری بودن آن است.
همچنین اشاره ی ظریفی به تنوع در باتری لیتیوم هوا Lithium air battery، بر اساس اکسیدهای مختلف لیتیوم صورت گرفته است که در بحث تنوع الکترولیت، بیشتر به آن خواهیم پرداخت.
مقایسه ی انواع باتری
ساختار باتری لیتیوم هوا
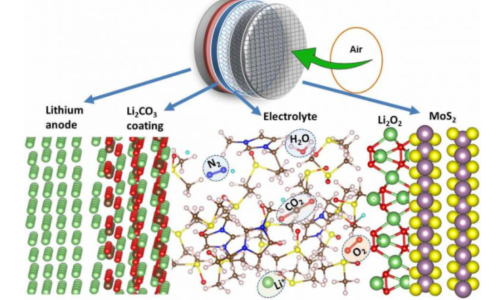
به عنوان یادآوری و مرور، اشاره می کنیم ساختار یک باتری لیتیم هوا، از آند لیتیومی با پوششی از کربنات لیتیوم تشکیل شده است. این پوشش، نقش مهمی در جلوگیری از رسوب روی آند و توقف عملکرد باتری و نیز اجتناب از واکنش بسیار شدید لیتیوم با آب می شود.
محیط الکترولیت، یک محیط آبی با حضور یون های لیتیوم، اکسیژن دریافتی از هوا و دی اکسید کربن ناشی از پوشش آندی می باشد. کاتد عملا هوا است که اکسیژن لازم برای اکسید شدن لیتیم را تامین می کند. اما به پوششی از جنس اکسید لیتیوم و سولفور مولیبدن به صورت متخلخل نیاز می باشد.
ساختار یک باتری لیتیوم هوا
شارژ و دشارژ باتری هوا
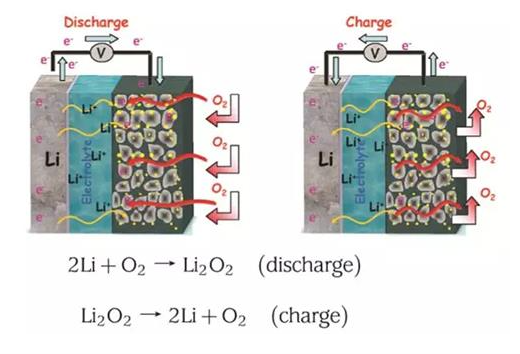
اساس کار باتری لیتیوم هوا، مشابه هر باتری فلز هوای دیگر، عبارت است از اکسید شدن لیتیم با اکسیژن دریافتی از هوا در مسیر دشارژ یا تخلیه و نیز فرایند احیا و آزاد شدن لیتیوم خالص و باز گرداندن اکسیژن به هوا، با دریافت انرژی از منبع خارجی در مسیر شارژ یا بارگیری. این موضوع به وضوح در شکل زیر نمایش داده شده و معادلات کلی شیمیایی نگارش شده است.
البته این معادلات شیمیایی، نتیجه ی کلی است و زیر معادلات یونی، بار الکتریکی و شیمیایی وجود دارد. ماحصل آن، عملکرد این سلول شیمیایی و تحویل یا دریافت انرژی در دشارژ و شارژ است. الکترولیت همواره مملوّ از یون های لیتیوم مثبت است با این تفاوت که تراکم آنها در مجاورت آند و کاتد در شرایط شارژ و دشارژ متفاوت است. رابطه ی معنا داری بین جهت دریافت و تحویل اکسیژن، با جهت حرکت الکترون ها (جریان الکتریکی) وجود دارد.
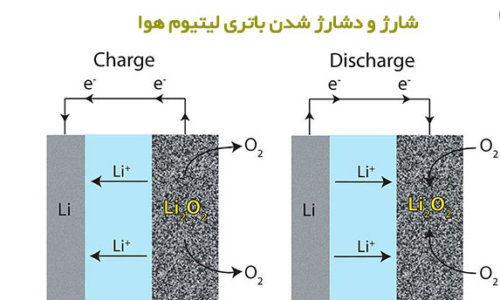
شارژ و دشارژ باتری لیتیوم هوا
هر چند در برخی شماتیک ها نظیر شکل زیر، جهت حرکت یون های لیتیوم مثبت در الکترولیت، در فرایند شارژ و دشارژ معکوس رسم شده است. اما مملوّ بودن الکترولیت از یون مثبت و صرفاً تراکم آندی یا کاتدی، معقول تر به نظر می رسد. ثابت بودن اکسید لیتیوم در سمت کاتد، بیان کننده ی پوشش و پوسته ی متخلخل هماهنگ با الکترولیت است و هوا، مطلقا تنها کاتد این باتری است.
ساختار باتری لیتیوم هوا
مروری بر انواع الکترولیت ها باتری لیتیوم هوا
در ادامه ی بحث، موضوع بسیار مهم تنوع الکترولیت در باتری لیتیم هوا Lithium air battery، مطرح می گردد. چهار نوع الکترولیت برای این باتری فلز هوای مبتنی بر لیتیوم مفروض است که به ترتیب، غیر آبی، آبی، هیبریدی و جامد می باشند. وجود هوا به عنوان تامین کننده اکسیژن، فلز آندی لیتیوم، کاتالیست از مشترکات هر چهار رویکرد می باشد و تفاوت در نحوه ی پیاده سازی الکترولیت می باشد.
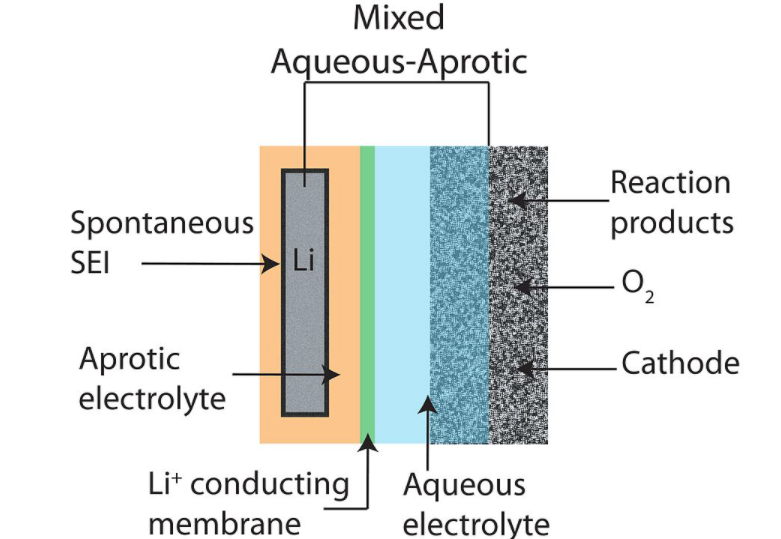
در الکترولیت غیر آبی، یک سیال آلی جای خود را به الکترولیت آبی می دهد. کربن متخلخل، معبر ورود هوا به کاتد را عهده می گیرد. در الکترولیت آبی، مواد آلی به سمت پوشش باتری در قسمت معبر ورود هوا می روند. همچنین یک لایه، بین آب و فلز لیتیوم حائل می شود تا مانع از واکنش شدید شود.
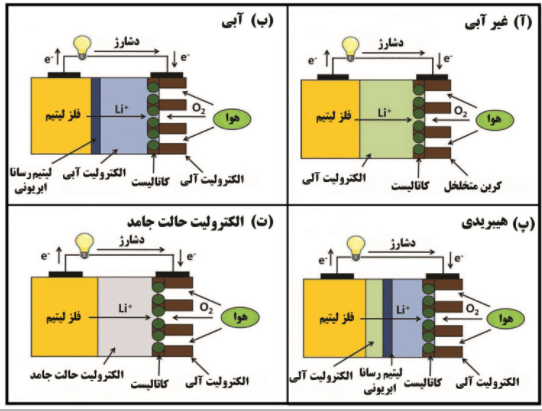
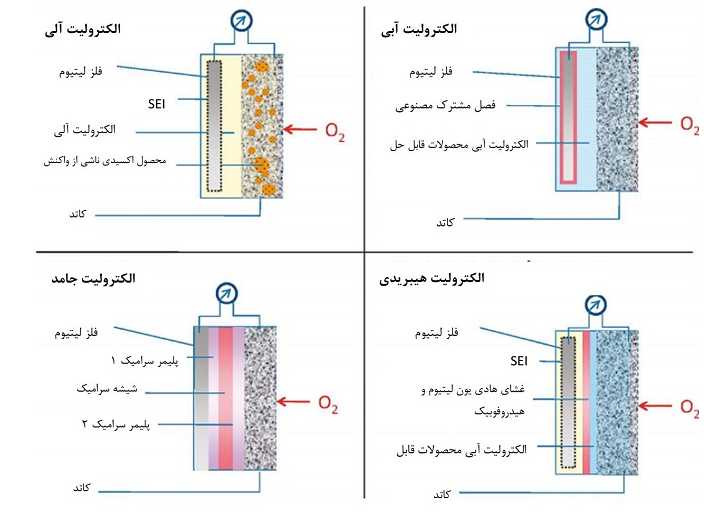
در رویکرد هیبریدی، کمی الکترولیت آلی در مجاورت فلز لیتیوم قرار می گیرد. سپس یک لایه حائل و بعد از آن الکترولیت آبی برای تبادل اکسیژن با هوای بیرون تعبیه می شود. در چهارمین رویکرد، اثری از سیال آلی یا آبی نیست. الکترولیت به صورت جامد پیاده سازی می شود. در شکل زیر این چهار رویکرد در پیاده سازی الکترولیت نمایش داده شده است.
چهار رویکرد در پیاده سازی الکترولیت
الکترولیت آبی
مهمترین مشکل رویکرد الکترولیت آبی در باتری لیتیوم هوا Lithium air battery، عدم قابلیت شارژ مجدد می باشد. هر چند معادلات بر روی کاغذ بازگشت پذیر می باشند، اما پیاده سازی موفق و قابل تجاری سازی مشاهده نشده است.
هیدروکسید لیتیوم در این رویکرد تولید شده و احیای فلز لیتیم در مرحله ی شارژ ولو با دریافت انرژی، میسر و سهل نیست. در این رویکرد نمک لیتیوم محلول در آب، به عنوان الکترولیت در نظر گرفته می شود. مخاطرات واکنش شدید لیتیوم با آب نیز در این رویکرد وجود دارد. لذا یک فصل مشترک مصنوعی در اطراف آند لیتیمی لازم است.
الکترولیت آبی
الکترولیت آلی
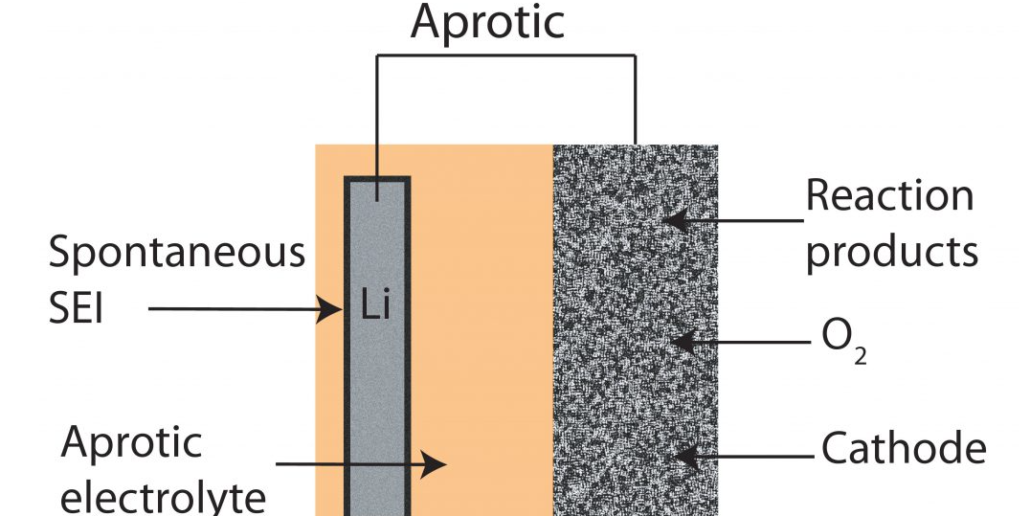
در رویکرد الکترولیت آلی، قابلیت شارژ تامین شده و ایمنی تا حد بالایی لحاظ می گردد. چرا که امکان واکنش شدید آب با فلز لیتیم با آسیب دیدن لایه ی فصل مشترک مصنوعی، وجود نخواهد داشت. محصول این نوع Lithium air battery، اکسید لیتیم بوده که با دریافت انرژی، قابل احیا است. اما مشکل دیگر، رسوب و عدم انحلال این اکسید است.
عملا هر دو نوع اکسید لیتیوم با ظرفیت های فلزی مختلف تولید می شود. در این رویکرد نیازی به لایه پوشش مصنوعی برای فلز لیتیم نیست.
الکترولیت غیر آبی یا آلی
الکترولیت هیبریدی
در رویکرد هیبریدی، همزمان الکترولیت آبی در مجاورت کاتد هوایی وجود دارد. همچنین الکترولیت آلی در مجاورت فلز لیتیوم در آند مستقر شده است. به عبارتی از مزایای هر دو الکترولیت استفاده شده است. در عین حال با استفاده از یک غشای مناسب، از معایب این دو الکترولیت خصوصا در مجاورت آند با آب و نیز اکسید لیتیوم با کاتد پرهیز می شود.
این غشا برای عبور یون لیتیم مثبت، رسانا است. در این رویکرد، قابلیت شارژ وجود دارد و خطر واکنش شدید فلز لیتیوم با آب نیست. اساسا در مجاورت آند لیتیومی، آب و الکترولیت آبی وجود ندارد. از سوی دیگر، رسوبات اکسید لیتیوم، تخلخل کاتد را از بین نمی برد؛ چون الکترولیت آلی در مجاورت کاتد نیست و اطراف آن را الکترولیت با محلول نمک لیتیم در آب فرا گرفته است.
الکترولیت هیبریدی
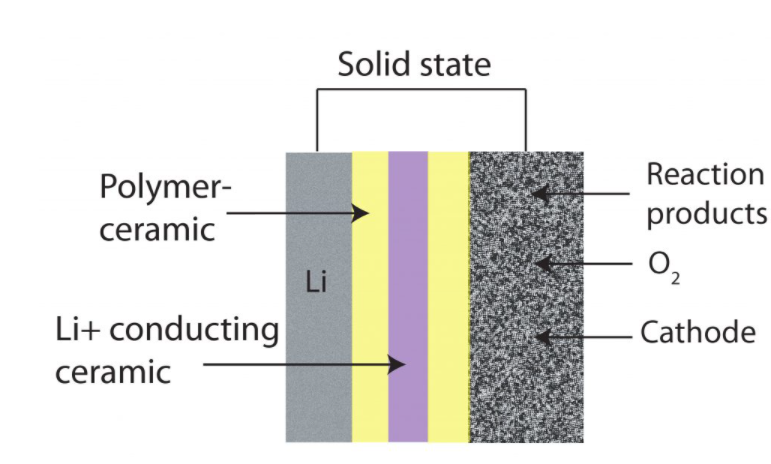
الکترولیت جامد
در رویکرد چهارم، الکترولیت به صورت جامد پیاده سازی شده است. از پلیمر سرامیک برای انتقال یون لیتیوم مثبت استفاده می شود. تا 30 سیکل شارژ و دشارژ موفق در ویرایش الکترولیت جامد، ثبت گردیده است.
در شکل زیر چهار رویکرد مختلف در تنوع الکترولیت نمایش داده شده است.
چهار رویکرد الکترولیت
پیاده سازی کاتد Lithium air battery
اکنون که قدری در خصوص الکترولیت باتری لیتیوم هوا بررسی صورت گرفته است، اشاره به نکاتی در خصوص کاتد و پیاده سازی آن نیز خالی از لطف نیست. کاتد در باتری های فلز هوا، با کربن فعال پیاده سازی می شود. به هر حال صرف بودن کربن، سبب پدید آمدن دی اکسید کربن محلول در الکترولیت می شود. در صورت وجود کلسیم، رسوب سخت و مشکل ساز کربنات کلسیم دور از ذهن نیست.
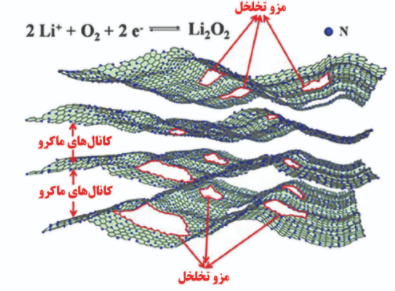
استفاده از فلزات گرانبها مانند طلا، نقره، پلاتین، پالادیوم، ایریدیوم عالی است اما هزینه ها را به طرز وحشتناک افزایش می دهد. استفاده از مس و کبالت اخیراً پیشرفت قابل ملاحظه ای داشته است. اکسید کبالت نیز، نتایج مطلوب و ارزانی را در بر داشته است. در شکل زیر راهکارهای پیاده سازی کاتد نمایش داده شده است.
راهکارهای پیاده سازی کاتد متخلخل
چالش های باتری لیتیم هوا
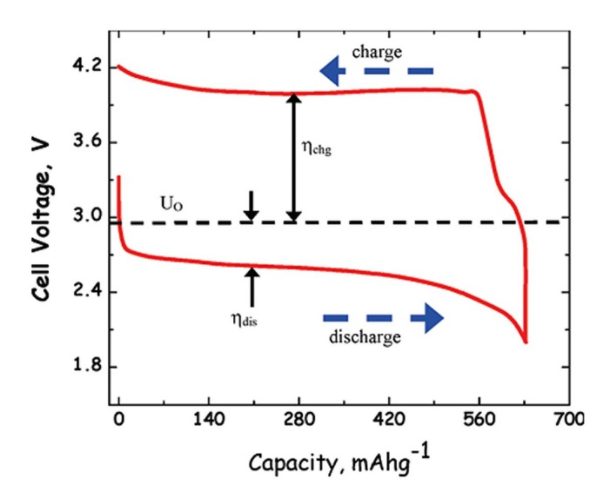
چالش های اصلی حل نشده یا به بلوغ فناوری نرسیده در حوزه ی باتری لیتیوم هوا، مسدود شدن آند و کاتد با ذرات و رسوبات دندریت مانند اکسید فلزات است. موضوع پلاریزاسیون و اور – پتانسیل سبب می شود سیکل شارژ و دشارژ، متقارن نبوده و نوعی از back Lash وجود داشته باشد و تعداد سیکل های موفق را کاهش دهد. در شکل زیر یک سیکل به همراه پیک های اور- پتانسیل نمایش داده شده است.
اور – پتانسیل ناشی از پلاریزاسیون
طبق شکل، مسیر شارژ از ولتاژی در حدود 1.8 ولت آغاز شده و خیلی زود به 4.2 ولت می رسد. به مجرد آغاز فرایند دشارژ، این ولتاژ به 3.3 ولت افت می کند.
پس از افت شدید دوم، به 2.7 ولت می رسد و تا اتمام دشارژ تقریبا ثابت می ماند اما این ولتاز تقریبا ثابت را نمی توان به عنوان ولتاژ تعادلی یاد کرد؛ عملا ولتاژ تعادلی، طبق شکل بالا، حدود 3 ولت در نظر گرفته می شود.
جمع بندی
به هر حال باتری لیتیم هوا، با توجه به ظرفیت ویژه ی انرژی خود اینقدر خوب است که محققین در فازهای آزمایشگاهی و نیمه صنعتی، در پی رفع چالش ها و موانع تولید این باتری با سیکل های متعدد و تقریبا نامحدود شارژ و دشارژ هستند. مشکل زمان شارژ طولانی باید حل شود و بهترین و ارزان ترین الکترولیت ها و کاتد ها، پیاده سازی شوند.
خوشبختانه نگرانی در خصوص محیط زیست نیست و باتری لیتیوم هوا دوستدار محیط زیست است. با اجتناب از الکترولیت آبی، تا حد زیادی مخاطرات استفاده از این نوع باتری ناشی از واکنش احتمالی شدید بین فلز و آب رفع شده و با تامین شدن ایمنی یا Safety، عملا باتری لیتیوم هوا یک محصول منطبق بر HSE(Health – Safety – Environment) خواهد بود.
این ارزش در کنار ظرفیت ویژه انرژی معادل 5 برابر باتری یون لیتیومی، ولتاژ 2.91 نامی رگولار ایده آل خواهد بود. هرگاه در خصوص ارزش باتری فلز هوای مبتنی بر لیتیوم نیاز به یادآوری داشتید، کافی است بدانید ظرفیت انرژی بنزین به عنوان یک سوخت همه گیر از مرتبه ی 49.8 ژول بر کیلوگرم است. این در حالی است که لیتیوم در باتری فلز هوا ظرفیتی معادل 40.1 را تامین می کند.
بنزین 13 کیلووات ساعت بر کیلوگرم تامین توان الکتریکی معادل می کند. این در حالی است که باتری فلز هوای لیتیومی، 12 واحد را تامین خواهد نمود. بی جهت نیست که باتری فلز هوای مبتنی بر لیتیوم را یک پیل سوختی تنفس کننده با هوا می نامند ! که البته این گزاره در مورد انواع باتری های فلز هوا صادق می باشد.






تعقیب
[…] باتری لیتیم هوا […]
[…] ساختار باتری لیتیوم هوا […]
دیدگاه خود را ثبت کنید
تمایل دارید در گفتگوها شرکت کنید؟در گفتگو ها شرکت کنید.